Небольшой беспорядок никогда никого не убивал, верно? Неправильно. Исследователи из Токийского медицинского и стоматологического университета (TMDU) недавно показали, что накопление клеточного "мусора" в мозге действительно может вызвать нейродегенерацию и даже смерть.
Сообщая о своих находках в Nature Communications, исследователи описывают, как дефекты в механизме удаления клеточных отходов, называемом "альтернативной аутофагией", могут привести к смертельному накоплению железа и белка в клетках мозга.
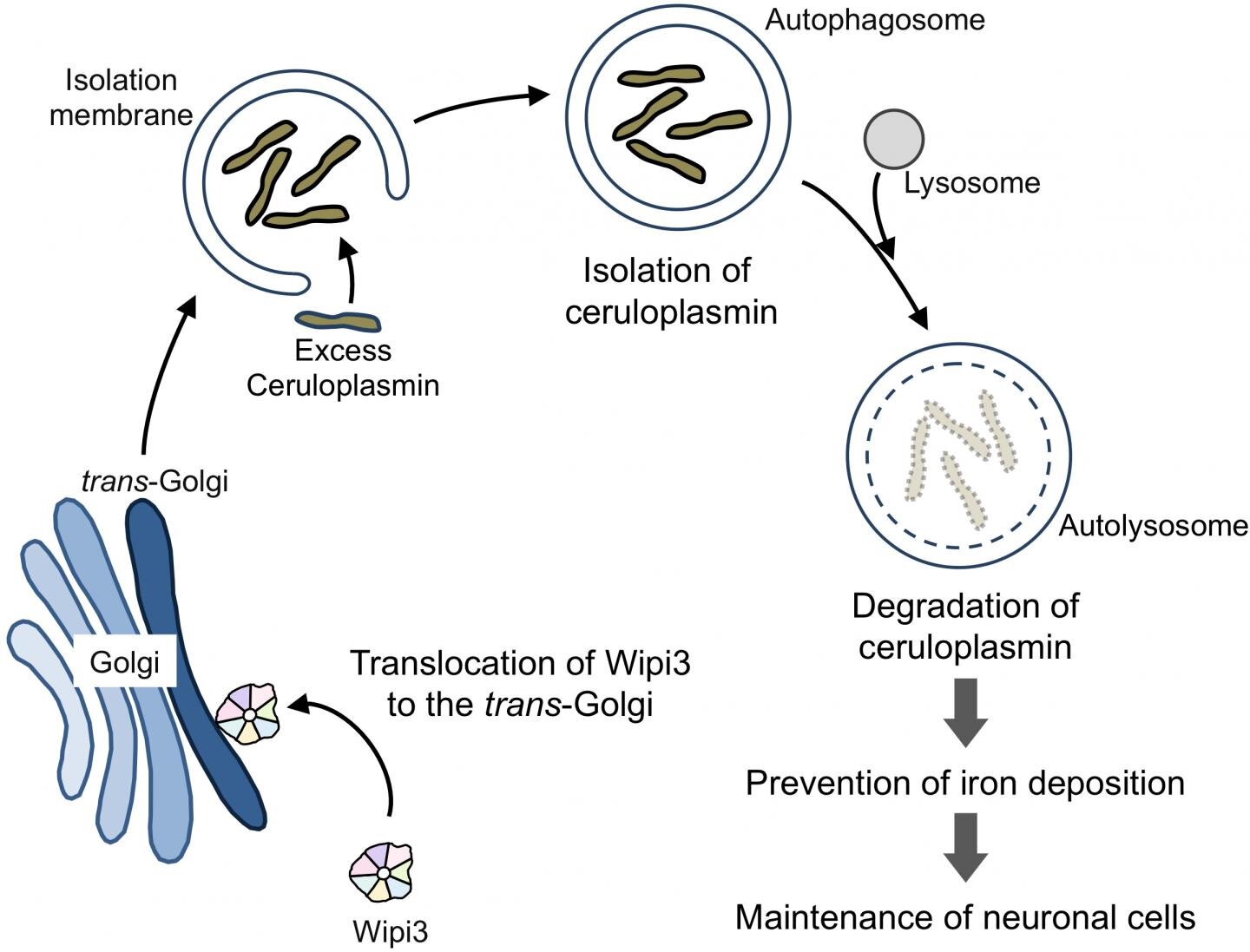
"Клетки постоянно очищаются от дисфункциональных или ненужных компонентов, которые затем разлагаются и перерабатываются", - объясняет ведущий автор исследования Хирофуми Ямагути. -Аутофагия-это процесс, при котором нежелательные клеточные компоненты и белки содержатся в сферическом пузыре с двойной мембраной, называемом аутофагосомой, который сливается с заполненной ферментами лизосомой, образуя аутолизосому. Затем отходы расщепляются и повторно используются клеткой."
Эта распространенная форма аутофагии, называемая канонической аутофагией, хорошо охарактеризована и включает набор связанных с аутофагией белков, таких как Atg5 и Atg7. Однако совсем недавно было также описано несколько независимых от Atg5 альтернативных путей аутофагии, биологическая роль которых остается неясной.
После выявления альтернативных белков, связанных с аутофагией в дрожжах, команда TMDU сосредоточилась на ортологе млекопитающих под названием "Wipi3", который ранее был вовлечен в каноническую аутофагию. "Когда мы удалили Wipi3 в клеточной линии мыши и индуцировали альтернативную аутофагию, мы больше не наблюдали образования двухмембранных аутофагосом или одномембранных аутолизосом, подтверждая, что Wipi3 необходим для альтернативной аутофагии", - говорит Ямагучи.
Мыши, содержащие специфичную для мозга делецию Wipi3, демонстрировали дефекты роста и моторики, наиболее часто наблюдаемые у пациентов с нейродегенерацией, причем исследователи также отмечали накопление железа и метаболизирующего железо белка церулоплазмина в клетках мозга пораженных мышей.
"Отложение железа было отмечено как возможный триггер при различных нейродегенеративных расстройствах и обычно связано с аномальным накоплением железосвязывающих белков",-объясняет старший автор исследования Сигеоми Симидзу. "Наши результаты являются убедительным доказательством того, что альтернативная аутофагия, и в частности Wipi3, может быть необходима для предотвращения этого токсичного накопления железа."
Интересно, что хотя мыши с дефицитом Wipi3 и Atg7 (каноническая аутофагия) демонстрировали сходные двигательные дефекты, они демонстрировали очень разные субклеточные изменения, предполагая, что альтернативная аутофагия и каноническая аутофагия действуют независимо для защиты нейронов. В подтверждение этого делеция как Wipi3, так и Atg7 у мышей почти всегда приводила к летальному исходу.
Исследователи надеются, что это исследование может привести к разработке нейропротекторных препаратов. Предварительные тесты показывают, что чрезмерная экспрессия Dram1, другого альтернативного белка, связанного с аутофагией, может обратить вспять эффекты делеции Wipi3 и может лечь в основу будущих методов лечения различных нейродегенеративных заболеваний. Статья "Wipi3 необходим для альтернативной аутофагии, и его потеря вызывает нейродегенерацию" была опубликована в журнале Nature Communications. | |
| Просмотров: 474 | |