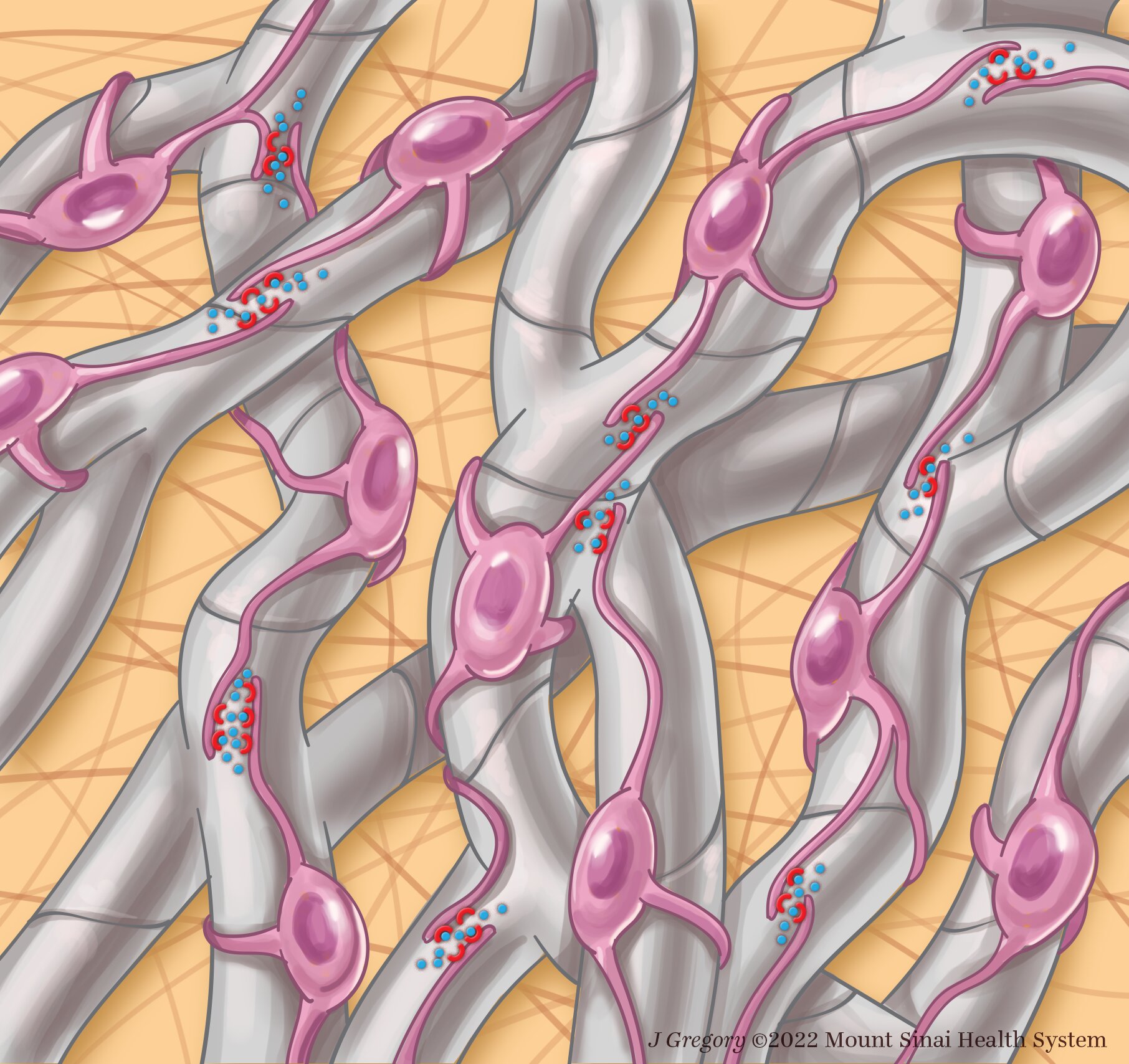
Используя новейшие технологии, включая одноядерное секвенирование тканей печени мышей и человека и передовую 3D визуализацию мышей на стекле для характеристики ключевых клеток печени, продуцирующих рубцы, исследователи обнаружили новые кандидаты в мишени для лекарств от неалкогольной жировой болезни печени (НАЖБП). Исследование проводилось под руководством ученых из Медицинской школы Икан при Маунт-Синай. Используя эти инновационные методы, исследователи обнаружили сеть межклеточной коммуникации, которая приводит к рубцеванию печени по мере развития заболевания. Результаты исследования, опубликованные 4 января в журнале Science Translational Medicine, могут привести к разработке новых методов лечения.
Заболевание NAFLD, характеризующееся отложением жира в печени и часто связанное с диабетом 2 типа, гипертонией и повышением уровня липидов в крови, представляет собой угрозу для всего мира. В США, по оценкам, этим заболеванием страдают от 30 до 40 процентов взрослых, причем около 20 процентов из них имеют более продвинутую стадию, называемую неалкогольным стеатогепатитом, или НАСГ, которая характеризуется воспалением печени и может прогрессировать до рубцевания (цирроза) и печеночной недостаточности. NASH также является самой быстрорастущей причиной рака печени во всем мире. Поскольку продвинутые стадии НАСГ вызваны накоплением фиброза или рубцов, попытки блокировать фиброз находятся в центре усилий по лечению НАСГ, однако в настоящее время нет лекарств, одобренных для этой цели, говорят исследователи. В рамках экспериментов исследователи провели одноядерное секвенирование в параллельных исследованиях как мышиных моделей NASH, так и тканей печени человека от девяти человек с NASH и двух контрольных. Они выявили общее число 68 пар потенциальных лекарственных мишеней для двух видов. Кроме того, исследователи проверили одну из этих пар, испытав на мышах существующий противораковый препарат в качестве доказательства концепции. "Мы стремились понять основу этого фиброзного рубцевания и определить лекарственные мишени, которые могут привести к новым методам лечения прогрессирующей НАСГ, изучая печеночные звездчатые клетки, которые являются ключевыми клетками, продуцирующими рубцы в печени", - сказал старший автор исследования Скотт Л. Фридман, доктор медицины, профессор медицины, декан по терапевтическим открытиям и заведующий отделением заболеваний печени в Икан Маунт Синай. "Сочетая этот новый подход к визуализации стеклянной печени - передовой метод очистки тканей, позволяющий получить глубокое представление - вместе с анализом экспрессии генов в отдельных звездчатых клетках, мы открыли совершенно новое понимание того, как эти клетки создают рубцы по мере развития NASH на поздних стадиях". Исследователи обнаружили, что на поздних стадиях заболевания стеллатные клетки развивают плотную сеть, или сетку, взаимодействий между собой, которые способствуют возникновению 68 уникальных пар взаимодействий, ранее не выявленных при этом заболевании. "Мы подтвердили важность одной из таких пар белков, NTF3-NTRK3, используя молекулу, уже разработанную для блокирования NTRK3 в раковых опухолях человека, и перепрофилировали ее, чтобы установить ее потенциал в качестве нового препарата для борьбы с фиброзом при НАСГ", - сказал первый автор Шуанг (Самми) Ванг, доктор философии, преподаватель Отдела болезней печени. "Это новое понимание развития фиброза предполагает, что прогрессирующий фиброз может иметь уникальный репертуар сигналов, ускоряющих рубцевание, которые представляют собой ранее не распознанный набор лекарственных мишеней". Исследователи предполагают, что схема взаимодействия клеток друг с другом развивается по мере прогрессирования заболевания, поэтому одни препараты могут быть более эффективными на ранних стадиях, а другие - на более поздних. И одно и то же лекарство может не работать на всех стадиях заболевания. В настоящее время исследователи работают с химиками из Icahn Mount Sinai над дальнейшей оптимизацией ингибиторов NTRK3 для лечения фиброза печени. Далее исследователи планируют провести функциональный скрининг всех кандидатов-интеракторов в системе клеточных культур, а затем протестировать их в доклинических моделях заболеваний печени, как это было сделано для NTRK3. Кроме того, они надеются расширить свои усилия, чтобы определить, лежат ли подобные взаимодействия между фиброгенными клетками в основе фиброза других тканей, включая сердце, легкие и почки. Статья называется "Аутокринная сигнальная цепь в печеночных звездчатых клетках лежит в основе прогрессирующего фиброза при неалкогольном стеатогепатите". | |
| Просмотров: 157 | |