Новые результаты создают платформу для более эффективных, селективных и чувствительных ДНК-биосенсоров, которые могут быть использованы для обнаружения различных патогенов и заболеваний. Электрохимические ДНК-биосенсоры имеют большие перспективы для мониторинга различных заболеваний. В целом, область их применения обширна: от целевых ДНК-аналитов, таких как бактериальные гены и опухолевые последовательности, до клинически значимых концентраций биомаркеров SARS CoV-2, например. Однако добиться надлежащей чувствительности и селективности таких систем и обеспечить их перенос из лаборатории в клиническую среду довольно сложно, поскольку эти подходы часто связаны со сложными химическими реакциями, электрохимической маркировкой, технически сложными материалами или многоэтапной обработкой.
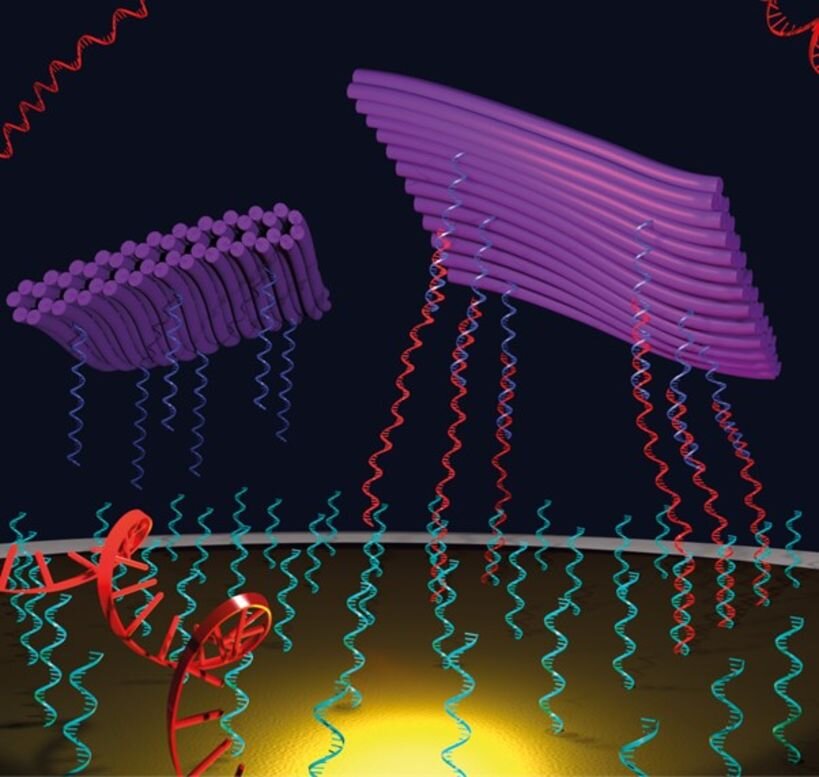
Теперь группа исследователей из Университета Аалто (Финляндия) и Университета Стратклайд (Глазго, Великобритания) нашла способ значительно повысить чувствительность электрохимических ДНК-датчиков, используя модульные наноструктуры ДНК в качестве их новых компонентов. Исследователи объединили традиционные методы создания датчиков на основе ДНК с программируемыми структурами ДНК-оригами для создания безметочного датчика со значительно увеличенной селективностью и чувствительностью обнаружения. "На практике наша отправная точка - это довольно простой и распространенный тип ДНК-биосенсора: мы имеем электродную систему, погруженную в раствор аналита, где чувствительный электрод покрыт одноцепочечными нитями ДНК-зонда, которые комплементарны (одноцепочечным) последовательностям целевой ДНК. Когда целевая нить связывается и гибридизуется с нитью зонда, электрические заряды вблизи электрода немного перемещаются, что означает, что мы можем увидеть изменение электрохимического сигнала", - объясняет докторант Петтери Пискунен из Университета Аалто, один из авторов исследования. "Здесь в игру вступают наноструктуры ДНК-оригами. Мы оснастили наши ДНК-оригами в виде плитки нитями захвата мишени, которые могут эффективно и избирательно связываться с одним концом последовательности мишени, в то время как другой конец мишени связывается с нитями зонда. Таким образом, мы создаем сэндвич-подобный комплекс, в котором целевая нить оказывается зажатой между электродом и ДНК-оригами. Тогда вместо регистрации небольшого изменения сигнала при связывании мишени мы увидим усиленный эффект из-за присутствия сравнительно большой ДНК-оригами", - продолжает Пискунен. "Мы продемонстрировали осуществимость нашей системы, обнаружив фрагмент гена из бактерий с устойчивостью к антибиотикам. Мы смогли селективно уловить эту цель из довольно сложного раствора, содержащего различные типы одноцепочечной ДНК, от коротких нитей и мусорных фрагментов до длинной циркулярной ДНК. С помощью нашего датчика мы смогли надежно обнаружить в 100-1000 раз меньшие концентрации мишени, чем при использовании традиционных методов", - говорит приглашенный ученый Вейкко Линко (в настоящее время доцент Тартуского университета, Эстония). "Обнадеживает мысль о том, что, сочетая универсальное ДНК-оригами, например, с печатаемыми и одноразовыми электродами, мы можем создать безметочные сенсорные платформы с такой высокой чувствительностью и специфичностью. Это открывает перед нашей технологией путь к массовому производству и широкому применению в качестве устройств для оказания медицинской помощи". В настоящее время совместно с Университетом Стратклайда ведется совместная работа по обобщению системы датчиков для использования с различными видами биомаркеров", - заключает Линко. Результаты исследования опубликованы в журнале ACS Sensors. | |
| Просмотров: 165 | |